2019年8月26日,国家药品监督管理局(以下简称国家药监局)发布《医疗器械唯一标识系统规则》,旨在贯彻落实国务院办公厅关于印发《治理高值医用耗材改革方案》的通知和《医疗器械监督管理条例》, 进一步加强医疗器械全生命周期的监督管理,创新监管模式。
医疗器械唯一标识(Unique Device Identifier,UDI)是医疗器械产品的身份证号码,可实现全链条医疗器械通查通识,是加强全生命周期管理,提升监管效能的重要手段。医疗器械唯一标识,是对医疗器械进行唯一性识别的一组代码,它由产品标识(Device Identifier,DI)和生产标识(Production Identifier,PI)组成,DI部分记录与产品相关的静态信息,PI部分记录与生产过程相关的动态信息,UDI与数据载体、数据库共同组成UDI系统。目前UDI已成为解决医疗器械全球监管问题的通用语言、国际语言和专业语言。在全球范围内,美国、欧盟、沙特阿拉伯、韩国等国家和地区已经发布UDI相关的法规和指导性文件,日本、澳大利亚、阿根廷等国家也相继开展了相关工作。2019年7月,国家药监局会同国家卫生健康委联合印发《医疗器械唯一标识系统试点工作方案》,我国UDI系统建设拉开了序幕;同年10月,国家药监局印发《关于做好第一批实施医疗器械唯一标识工作有关事项的通告》,对第一批医疗器械UDI实施的品种范围、进度安排、工作要求等进行了明确规定;2020年9月国家药监局印发《关于深入推进试点做好第一批实施医疗器械唯一标识工作的公告》,进一步拓展医疗器械唯一标识在医疗、医保等领域的衔接应用;2021年9月国家药监局印发《关于做好第二批实施医疗器械唯一标识工作的公告》,在前期工作的基础上将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围,支持和鼓励其他医疗器械品种实施唯一标识;2023年2月国家药监局印发《关于做好第三批实施医疗器械唯一标识工作的公告》,进一步贯彻落实和深化医药卫生体制改革重点工作任务。建立UDI系统,有助于提升企业信息化管理水平,建立产品追溯体系,提升企业管理效能,助推医疗器械产业高质量发展,有助于流通企业建立现代化物流体系,实现医疗器械供应链的透明化、可视化、智能化,有助于医疗机构加强医疗器械在临床使用环节的风险管控,降低器械使用差错率,保障患者用械安全,有助于医疗器械监管部门构建器械监管大数据,实现对医疗器械的来源可查、去向可追、责任可究,实现智慧监管,有助于提升卫生、医保、海关等部门对于医疗器械临床使用、招标采购、医保结算、进口通关等环节的管理效率,有助于社会公众放心用械、明白消费。
标签选择
UDI标签的印制质量对UDI编码的快速、准确识读至关重要,标签应当满足自动识别和数据采集技术以及人工识读的要求,只有确保UDI标签印制合格,才能切实保障UDI系统的有效实施。医疗器械生产企业应当对UDI标签进行定期检测,确保UDI符号的印制质量符合国家标准和客户要求,尤其是出口产品,还应符合出口国家的相关质量要求。
GS1标准的UDI数据载体有三种形式,分别是一维条码(EAN-13、GS1-128等)、二维码(GS1 DataMatrix)和射频识别(Radio Frequency Identification,RFID)标签,实际应用中推荐采用GS1-128码或GS1 DataMatrix码,如图1所示。
图1 条码标签示例图
UDI标签的检测
码制检测
对GS1-128码制进行检测,检测其是否被误用为Code 128码制。GS1-128码制是普通128码制的子集,由GS1和国际自动识别与移动技术协会(Association for Automatic Identification and Mobility,AIM Global)授权,将128条码起始符号后面的第一个字符值“FNC1”指定给GS1使用,因此,GS1-128条码拥有特殊的双字符起始符号:Start(A或B或C)FNC1,这种特殊的起始符号区分了GS1-128码和普通的Code 128码。GS1-128码制具有更高的安全性,并且可以更好的区分GS1系统的单元数据串与其他非标准的条码符号。
对GS1-DataMatrix码制进行检测,检测其是否被误用为Data Matrix Code、QR Code或GS1 QR Code码制。GS1标准体系中有GS1 DataMatrix Code和GS1 QR Code两种二维码载体标准,但是为了提高医疗供应链各参与方扫码的效率和准确性,在医疗产品标识选择二维码时,GS1医疗只推荐使用已在全球医疗产品包装上广泛使用的GS1 DataMatrix Code,不应使用GS1 QR Code。
GS1 DataMatrix Code具有物理形态小、信息密度高、可以采用多种方法在不同基底上印制等特性,在空间有限条件下标记单个产品部件的理想解决方案。
编码结构检测
UDI编码数据包括产品标识DI和生产标识PI,GS1标准的医疗器械产品标识为全球贸易项目代码(Global Trade Item Number,GTIN),我国主要采用的GTIN包括GTIN-13或GTIN-14标识代码,生产标识是由应用标识符(Application Identifier,AI)表示。当UDI中同时包含DI和PI时,需要在GTIN前增加应用标识符(01),当以人工识读形式呈现时,AI通常显示在括号中(括号并不是条码编码数据的一部分),根据监管和实际应用需求,可包含医疗器械序列号AI(21)、生产批号AI(10)、生产日期AI(11)、失效日期AI(17)等,括号中的内容为应用标识符AI,一般预定义长度AI放在前面,若在AI后的数据位数为可变长度,要在该数据后用FNC1来分隔数据。编码数据内容中的定长部分建议放在前面、变长部分放在后面,变长数据与定长数据之间、变长数据与变长数据之间需要用FNC1分隔字符进行分隔,从而提高译码效率。注意检测其编制是否符合规范要求,避免出现未加括号或自编等不符合要求的无效应用标识符。
模块(X尺寸)的宽度检测
在GS1-128条码中X尺寸指的是窄单元的标称值,它直接影响了条码符号的长度。在不同的应用场景中,GS1-128条码符号的X尺寸不同,见表1。
表1
GS1 DataMatrix中X尺寸指的是模块尺寸的标称值,它直接影响了条码符号的模块宽度。在不同的应用场景中,GS1 DataMatrix条码符号的X尺寸也不同,见表2。
表2
对条码符号的X尺寸进行检测,GS1-128码制与GS1-Datamatrix码制的X尺寸须分别满足表1和表2中X尺寸数据要求。GS1-128条码的X尺寸过小会导致条与空黏连在一起,识读设备无法区分出条与空,导致无法译码或可译码度太低。
空白区及条高检测
一维条码符号空白区的作用是提示识读设备两个空白区之间的扫描信号是有用的,应该被提取并译码;二维码符号空白区的作用是将其与周围的其他图形进行区分,便于识读设备精准确定译码区域。对条码空白区进行检测,空白区宽度过小会导致识读设备无法准确识读条码,因此空白区的宽度应不小于标准规定的最小尺寸,如图2所示。
图2 条码空白区不足
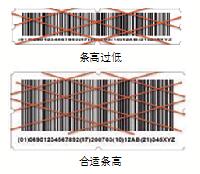
对GS1-128码制的条码高度进行检测,足够的条高是为了保证扫描识读的效率,条高过低或不符合符号高度的条码会导致扫描器识读性能降低,对于扫描效率高的全向扫描方式而言,符合要求的条码符号高度尤为重要;条高足够高时,识读设备不同角度的扫描线很容易贯穿整个条码符号,至少有一条可以经过所有的条和空,确保一次识读成功,如图3所示。
图3 条码扫描示例
供人识读字符一致性检测
根据国家药监局发布的《医疗器械唯一标识系统规则》(2019年第66号)第十一条的规定:医疗器械唯一标识数据载体应当满足自动识别和数据采集技术以及人工识读的要求。
检测供人识读字符(Human Readable Interpretation,HRI)部分是否与自动识别部分的数据内容一致,是否使用了清晰易读的字体(例如,ISO 1073-2中定义的OCR-B和《GS1通用规范》7.11中定义的字符集或其他字迹清晰的合理替代字体类型和字符大小)。HRI是否与条码有明确的关联性,打印位置应紧邻数据载体,且不能占用空白区,如图4所示。在应用过程中,如果供人识别字符与自动识别部分的内容不一致,使用者难以分辨两部分内容的正确性,从而影响医疗器械产品的流通速度和医疗器械唯一标识作用的发挥。
图4 标记HRI文本的数据标签
GS1-128条码长度和数据字符检测
对GS1-128条码长度进行检测,如果其最大物理长度超过165mm,或者数据字符个数超过48个,会导致其无法被识读或数据丢失,如图5、6所示。
图5 数据字符个数大于48个
图6 条码符号物理长度大于165mm
对于此类不合格问题,企业可以采用GS1-128条码“并联”(双行或多行)表示,如图7所示。
图7 GS1-128条码并联
条码印制质量检测
对GS1-128条码印制质量进行检测,检测其是否存在参考译码错误、可译码度太低、边缘反差太小、调制比太低、缺陷度太大等不合格因素。对GS1 DataMatrix的印制质量进行检测,检测其是否存在符号反差太小、轴向不一致性太高、固有图形污损太高、未使用的纠错太少、调制比、摸校调制比太低等不合格因素。企业要根据检测出的质量问题对印刷材料、打印设备、印刷条件(湿度、打印速度)等采取相应的改进措施及时调整工艺,确保GS1-128和GS1 DataMatrix的符号等级不低于1.5级,防止不合格的UDI数据载体进入流通领域,造成经济损失以及医疗事故。
条码放置位置检测
检测条码符号(包括空白区)是否放置在了有穿孔、冲切口、开口、接缝、折叠、折边、隆起或皱褶、曲率过大、太近边缘、交叠、波纹和纹理粗糙的地方,都会造成扫描障碍,导致识读困难甚至拒读问题的发生。对于手控扫描的过程,符号位置经常变化使扫描操作员难以预料符号处于何处,会降低扫描效率,而对于自动扫描过程,符号的位置必须恰当,以使其移过时通过固定式扫描器的视场。
商品条码位置的选择应以符号位置相对统一、符号不易变形、便于扫描操作和识读为准则,应符合GB/T 14257-2009《商品条码 条码符号放置指南》的要求。条码符号放置首选位置为项目背面的右侧下半部分的区域内,选择时还要考虑到条码符号四周的空白区和边缘原则(条码符号与商品包装临近边缘的间距不应小于8mm或大于100mm),项目背面以外的一个面的右侧下半部分区域内也可以作为可选位置。对于物流单元,条码符号放置位置应远离垂直边缘,防止条码符号在运输过程中受损。
条码照片拍摄及预处理
对待检测条码进行照片拍摄,要满足以下要求:
所拍摄照片应包括包装整体照片以及清晰可读的标签,确保标签能被机器准确识读,要保证充足的光源,避免所拍摄条码照片对比度过低。
对条码进行照片拍摄时可通过摆放合适的参照物来进行比对,例如可以按要求设计标准板作为拍摄参照物,标准板可以是符合要求的直尺或带刻度符号的水平板,将标准板与条码放置在同一平面上进行拍摄,确保摄像头垂直于条码所在平面,如果有需要,条码检测机构可以提供统一标准板作为拍摄参照。
条码图像在获取过程中,由于拍摄角度、成像系统非线性等原因,会产生比例失调,甚至产生畸变现象,畸变主要包括径向畸变和倾斜畸变两种。对径向畸变进行校正的代表性的方法有: 两步法、使用控制点的方法、基于摄像机模型的校正方法、变焦距地址修正法等。在倾斜畸变中,梯形畸变是最常见的畸变之一,可以采用控制点进行校正。
从成像设备得到的条码图像可能包含干扰以及光照不均匀现象,光照不均匀会严重影响条码的读取,导致后续译码的失败,对收到的条码图片进行预处理,采用合适的算法进行二值化处理,提高条码的识别率。
UDI系统将推动实现医疗器械智慧监管与社会共治,助力产业转型升级和健康发展,为公众提供更加安全高效的医疗服务,增强人民群众的获得感、幸福感和安全感。通过电子邮件或其他通讯方式进行UDI标签图片送检不但可以节约企业邮寄成本,提高资源利用率,更重要的是可以有效应对各种突发公共卫生事件,在医疗器械流入市场前从源头进行标准和安全把控,防患于未然。
单翔宇 姜磊磊 李乐
作者单位:江苏分中心
《中国自动识别技术》2023年第3期总第102期